
|
Σύμφωνα με τον Π.Ο.Υ (World +++ Health Organization. Global Tuberculosis Control 2010. WHO/HTM/TB/2010.7. Geneva, World Health Organization, 2010), η λοίμωξη από μυκοβακτηρίδιο της φυματιώσεως και η επακόλουθη νόσος η φυματίωση (ΤΒ), παραμένει μείζον αίτιο νοσηρότητας και θνησιμότητας, πλανητικής εμβέλειας και δεν έχει ακόμη, αναχθεί σε ιστορικής σημασίας ζήτημα, καθώς είναι γνωστό ότι το 2009 κατεγράφησαν 1.7 εκατ. θάνατοι, μεταξύ 2 δισεκατ. ατόμων που φέρονται με θετική Mantoux, απότοκη λανθάνουσας μολύνσεως. Σημειώνεται ετήσια αύξηση της επιπτώσεως κατά 2.7%, μεταξύ των ετών 2004-2008. Για τα άτομα αυτά, ο εφ΄όρου ζωής κίνδυνος να αναπτύξουν ενεργό νόσο είναι <10%, αλλά τυχόν έκπτωση της κυτταρικής άμυνας μπορεί να συντελέσει στη δραστική αύξηση του κινδύνου. Το σημαντικότερο αίτιο μειώσεως της κυτταρικής άμυνας είναι η λοίμωξη από ιό HIV και η διαρκώς αυξανόμενη επίπτωση του AIDS εισφέρει στην επέκταση της φυματιώσεως, καθώς, τα τελευταία 40 χρόνια 0.38 εκατ. θάνατοι έχουν καταγρφεί, που αφορούν ασθενείς με HIV+TBC. Ατυχώς, αυξανόμενη βαίνει, επίσης, και η επίπτωση των πολυανθεκτικών περιπτώσεων φυματιώσεως, καθώς αφορούν στο 3.6% όλων των νέων περιπτώσεων (εικόνα 1).
|
Ιστορία
πνευμονική φυματίωση
-
πρωτοπαθής πνευμονική φυματίωση
-
μεταπρωτοπαθής πνευμονική φυματίωση
-
κεγχροειδής πνευμονική φυματίωση
- φυματιώδης πλευρίτις
καρδιακή φυματίωση
φυματίωση του ΚΝΣ
-
φυματιώδης μηνιγγίτις
-
ενδοκρανιακό φυμάτωμα
-
ενδοκρανιακό απόστημα
-
φυματιώδης εγκεφαλοπάθεια
φυματιώδης ωτομαστοειδίτις
φυματιώδης μαστίτις
φυματιώδης λεμφαδενοπάθεια
-
τραχηλική λεμφαδενοπάθεια, scrofula
φυματίωση του εριστικού συστήματος
-
φυματιώδης σπνοδυλίτις, νόσος του Pott
-
φυματιώδης οστεομυελίτις
-
φυματιώδης αρθρίτις
φυματίωση του ΓΕΣ και φυματιώδης περιτονίτις
φυματίωση ουροποιογεννητικού συστήματος
-
φυματίωση των νεφρών
-
φυματίωση της ουροδόχου κύστεως
-
φυματίωση του προστάτη
-
φυματίωση των ανδρικών γεννητικών οργάνων (όρχεων, επιδιδυμίδας, του σπεραμτικού τόνου)
-
φυματίωση της γυνακείας πυέλου
-
φυμάτωμα
επιδημιολογία
παθογένεια
διάγνωση
διάγνωση ενεργού φυματιώσεως
HIV + TBC
Θεραπεία
πολυανθεκτική φυματίωση α'
πολυανθεκτική φυματίωση β'
διαθέσιμα αντιφυματικά φάρμακα
προτεινόμενα -νεα- φάρμακα, στη θεραπεία της ΤΒ
η χρήση των κορτικοστεροειδών
έλεγχος φυματιώσεως
επίλογος
Η φυματίωση στο διαδίκτυο
εισπνεόμενα γλυκοκορτικοειδή και φυματίωση
Σύμφωνα με εκτιμήσεις του Π.Ο.Υ. 1.72 δισεκατομμύρια άτομα (το 1/3 του παγκόσμιου πληθυσμού) έχουν ανενεργό λοίμωξη με το μυκοβακτηρίδιο της φυματιώσεως (μΦ), ενώ 15-20 εκατομμύρια έχουν ενεργό νόσο, ενώ καταγράφονται 3 εκατομμύρια θάνατοι από φυματίωση, το χρόνο (το 95% εξ αυτών στον αναπτυσόμενο κόσμο). Εκατό χρόνια νωρίτερα, στο ΗΒ πέθαναν περισσότερα από 30000 άτομα το χρόνο από φυματίωση, αριθμός που αντιστοιχεί με την τρέχουσα θνητότητα των πνευμονικών νεοπλασμάτων, σήμερα. Η θνητότητα και η επίπτωση της νόσου μειώνεται σταθερά, έκτοτε, λόγω της βελτιώσεως της διατροφής και των κοινωνικών συνθηκών και η ταχύτερη μείωση παρατηρείται μετά το τέλος της δεκαετίας του 1940, οπόταν διατέθηκε αποδοτική θεραπεία. Εν τούτοις, τελευταία, η μείωση της επιπτώσεως εμφανίζει στασιμότητα καθ΄όλη τη διάρκεια των τελευταίων δεκαετιών, ενώ παρατηρείται αύξηση σε σποραδικές περιοχές. Ενώ, π.χ., στο ΗΒ, η θνητότητα κυμαίνεται περί τους 5800 θανάτους κατ΄έτος, το 1987, αυξήθηκε στις 6500, πρόσφατα. Η αύξηση της επιπτώσεως της φυματιώσεως κυρίως εντοπίζεται στις μεγαλουπόλεις, και ο κίνδυνμος είναι ακόμη μεγαλύτερος στον μειονωτικό πληθυσμό που αναμιγνύεται στις μεγάλες πόλεις, λόγω της αθρόας προσελεύσεως οικονομικών μεταναστατών, οι οποίοι προέρχονται από χώρες με υψηλούς δείκτες διαμολύνσεως (ποσοστό ατόμων ηλικίας 17 ετών, με μεταστροφή της δερματικής δοκιμασίας στη φυματίνη, που δεν οφείλεται σε προηγηθέντα εμβολιασμό) ή λόγω των υποβαθμισμένων συνθηκών διαβιώσεως στις χώρες όπου φιλοξενούνται. Επιπλέον, περισσότερο επιρρεπείς είναι οι άστεγοί, οι χρόνιοι καταχραστές οινοπνεύματος και τα άτομα που έχουν μολυνθεί με τον HIV. Στο ΗΒ, 40% του επιπλοασμού εμπίπτει σε λευκούς, 40% σε άποικους αππο την Ινδία και 16% σε έγχρωμους. Η λοίμωξη μπορεί να συμβαίνει στην παιδική ηλικία και να πααμένει σιωπηλή επί χρόνια, πριν αναζωπυρωθεί. Στους παράγοντες που ευνοούν την αναζοπύρωση και την τη μείωση της αντιστάσεως έναντι του μΦ είναι η ηλικία, η κατανάλωση οινοπνεύματος, που συνοδεύει ή οφείλεται στη δυσθρεψία, την πτωχή διατροφή, την έκπτωση της κυτταρικής ανοσίας, λόγω άλλων παθήσεων ή των θεραπειών τους (π.χ., χημειοθεραπεία, ανοσοκατασταλτικά), και η συνοσηρότητα από λοίμωξη με HIV. Σε χώρες όπου η επικάλυψη μεταξύ της επιπτώσεως της μολύνσεως από ΗIV και της της μολύνσεως από ΜΦ έχει περιοριστεί, μόνο το 5% των ασθενών με ενργό επίκτητη ανοσοανεπάρκεια (AIDS) εμφανίζουν φυματίωση και μόνο 3% των ασθενών με φυματίωση ταυτοποιούνται ως φορείς του HIV. Εν τούτοις, εκτιμάται ότι 4.5 εκατομμύρια άτομα σε όλον τον κόσμο πάσχουν από φυματίωση και AIDS, 98% εξ αυτών σε αναπτυσσόμενες χώρες.
κλινική πορεία. Η κλινική πορεία της φυματιώσεως διαρκεί επί πολλά χρόνια, συνήθως, και παριστά πολύπλοκες αντεπιδράσεις μεταξύ του αμυντικού συστήματος (σύμφυτου και προσαρμοσμένου) του ξενιστού και του μΦ. Κατά παράδοση, η φυματίωση διακρίνεται σε δύο στάδια: την πρωτοπαθή φυματίωση και την μεταπρωτοπαθή. παρ΄όλο ότι αυτοί είναι χαρακτηρισμοί που αποδόθηκαν στην πορεία της νόσου πριν από την εποχή της διαθέσεως δραστικών αντιφυματιών φαρμάκων.
-πρωτοπαθής φυματίωση. Η πρωτοπαθής φυματίωση είναι η κορφή της νόσου που παρατηρείται κατά την πρώτη επαφή του ασθενούς με τη νόσο, που βρίσκει το άτομο χωρίς εγκατεστημένη ειδική άμυνα έναντι της φυματιώσεως. Η λοίμωξη συμβαλίνει με εισπνοή μικροοργανισμών που προήξλθαν από την εξώθησή τους από μολυνθέντα άτομο, με την αναπνοή, το βήχα, το γέλιο. Τα σταγονίδια που εκπέμπονται με την αναπνοή του πάσχοντος φέρουν μεγάλο αριθμό μΦ, τα οποία δεν αποσυντίθενται στο εξωτερικό περιβάλλον, αλλά παραμένουν, μεταφερόμενα επί των σωματιδίων της σκόνης, για μεγάλο διάστημα, σποροποιούμενα. Μετά την εισπνοή, η αρχική βλάβη τυπικά ανπτύσσεται στις υποπλεύριες περιοχές του πνεύμονος και ιδίως στους κάτω λοβούς, επειδή εκεί κυρίω κατευθύνεται το ποσόν του αέρος που εισπνέεται κατά την ήρεμη αναπνοή. Ακολουθεί κυψελιδίτιδα, λεμφαγγειΐτιδα και σύστοιχη, περιοχική λεμφαδενίτιδα, που ο έμπειρος κλινικός Ιατρός μπορεί να διακρίνει στην ακτινογραφία. Συγκεκριμένα στην ακτινογραφία θώρακος διακρίνεται το πρωτοπαθές σύμπλεγμα, ως μικρή, περιφερική περιοχή πυκνώσεςω (εστία του Gohn) και η πυλαία αδενίτιδα. Η κλινική εικόνα, στη φάση αυτή χαρακτηρίζεται από άτυπα αναπνευστικά συμπτώματα, νυκτερινούς ιδρώτες και απώλεια βάρους, αλλά η έντασή της κυμαίνεται από ήπια μέχρι πολύ σοβαρή, που απειλέι την ζωή του ασθενούς (π.χ., σύνδρομo Waterhouse-Friedman). Στις επόμενες τρείς εβδομάδες αναπτύσσεται ειδική ανοσοαπαντήση και η δερματική δοκιμασία με κεκαθαρμένη φυματίνη μεταστρέφεται σε θετική. Συνήθως, ακολούθως παράγεται έπούλωση' της αρχικής βλάβης, η οποία έκτοτε εμφανίζεται ως μικρό κοκκίωμα στη θέση της προηγθείσης εστίας του Gohn, ή εξαφανίζεται. Στο στάδιο αυτό, η νόσος είνια συνήθως ασυμπτωματική αν και μπορεί να καταλείπει αποτιτνωμένα οζίδια στην απλή ακτινογραφία θώρακος. Ενεργός εξέλιξη της πρωτοπαθούς βλάβης μπορεί, επίσης, να συμβεί, με βρογχική επέκταση των αθρόα παραγομένων μΦ και μπορεί να προκληθεί πύκνωση, που σύντομα υφίσταται τήξη και εμφανίζεται κοιλότητα. Παράλληλα, στη φάση αυτή αναγνωρίζεται πλευριτική συλλογή που προέρχεται είτε απ΄ευθείας μέσω εκβολής της κοιλότητας στην υπεζωκοτική κοιλότητα ή με βάση ανοσολογικούς μηχανισμούς. Και στις δύο περιπτώσεις πρόκειται περί λεμφοκυτταρικού εξιδρώματος, αλλά στην μεν πρώτη περιπτωση μπορεί η καλλιέργειά του να αποδώσει Μφ, ενώ στη δεύτερη δεν αναμένεται να αποβεί θετική. Η λεμφαγγειακή διασπορά της λοιμώξεως μπορεί να προκαλέσει διόγκωση των περιοχικών λεμφαδένων που στα αιδιά, λόγω ανωριομόττηας των βρογχικών τοιχωμάτων, μπορεί να προκαλέσει συμπίεση των βρόγχων, περιφερική πνευμονία, και να αναπτυχθούν βρογχεκτασίες εκ συμπιέσεως και ελλειπούς παροχετεύσεως, ή και σύνδρομο μέσου λοβού. Οι βρογχεκτασίες του μέσου λοβού είναι τυπικό εύρημα της πυλαίας αδενοπάθειας, από φυνατίωση της παιδικής ηλικίας.
εικόνα 4. |εικόνα 4|. η φυσική ιστορία της φυματιώσεως
Αιματογενής διασπορά. Η αιματογενής διασπορά πουακολουθεί την αρχική κυψελιδίτιδα (βλ. παραπάνω), απολήγει σε πρώιμη γενίκευση της φυματιώσεως και διασπορά σε πολλά όργανα και συστήματα, ανάλογα με την αιμάτωσή τους. Στον πνεύμονα, η τοπική διασπορά μπορεί να εξελιχθεί σε κεγχροειδή φυματίωση και στην δυνητικά θανατηφόρο, φυματιώση μηνιγγίτιδα, ιδιαίτερα στα μικρά παιδιά. Η διασπορά της λοιμώξεως σε αυτήν την πρώιμη φάση της, μπορεί να παραμείνει σιωπηλή για άλλοτε άλλα διαστήματα, ανάλογα και με την κυτταρική άμυνα του ξενιστή, σε διάφορα όργανα, στους πνεύμονες, τους νεφρούς τα οστά κλπ. απ΄όπου μπορεί να αναζωπυρωθεί. Εάν συμβεί αναζωπύρωση από τις εναποθέσεις της στους πνεύμονες, η αναζωπύρωση αναμένεται να εκδηλωθεί στα κορυφαία τμήματα των λοβών (άνω και κάτω), επειδή εκεί διατηρούνται ευνοϊκότερες συνθήκες για την επιβίωση του μΦ (λιγότερο οξυγόνο, λιγότερη αιμάτωση). -
μεταπρωτοπαθής φυματίωση. ||φυματίωση|
H μεταπρωτοπαθής φυματίωση είναι ο τύπος της φυματιώσεως που παρατηρείται μετά την ανάπτυξη της ειδικής, κυτταρικής άμυνας. Μπορεί να συμβεί κατ΄ακολουθία της μεταπρωτοπα0θούς, ή να συμβεί, μετά ενδογενή αναζωπύρωση της λοιμώξεως. Μπορεί, επιπλόεν, όμω,ς να συμβεί αναμόλυνση, οπότε τότε η νέα της εικόνα θα εδράζεται στις βάσδεις των πνευμόνων, εάν η μόλυνση είχε γίνει αερογενώς, πράγμα που είναι συνηθέστερο, στην εποχή μας της πλήρους πααστεριώσεως του γάλακτος. Η αναμόλυνση συνήθως παρατηρείται στους ηλικιωμένους, στους οποίους έχει μειωθεί η άμυνα του οργανισμού ή είναι ανοσοκατεσταλμένοι, λόγω συνοσηροτήτων ή λήψεως ανοσοκατασταλτικών φαρμάκων. Οι πνεύμονες είναι το συχνότερο όργανο που εμφανίζεται η μεταπρωτοπαθής φυματίωση, και, όπως προειπώθηκε, οι κορυθφές η συχνότερη εντόπισή της.
Η επίπτωση της φυματιώδους πλευρίτιδας ποικίλεισημαντικά από περιοχή σε περιοχή. Στις ενδημικές χώρες, η φυματίωση είναι το συχνότερο αίτιο πλευριτικής συλλογής. Η διάγνωση της φυματιώδουςς πλευρίτιδος αποδεικνύεται, συχνά, δυσχερής, για διάφορους λόγους. Η φυματιώδης πλευρίτις αναπτύσσεται ως επιβραδυνομένη αντίδραση υπερευαισθησίας, στις μυκοβακτηριαδιακές πρωτεΐνες κια ο μικροβιακός πληθυσμός στο πλευρτικό εξίδρωμα ελλείπει ή είναι χαμηλός, με αποτέλεσμα η καλλιέργεια πλευριτικού υγρού και ιστού να αποβαίνουν αρνητικές. Επιπλέον, η φ. πλευρίτις συχνά παραβλέπεται, επειδή στο 50% των ασθενών με πλευρίτιδα παριστούν πρωτοπαθή λοίμωξη, χωρίς νεδείεξις νοσηρότητας σε άλλα όργανα. Το πλευριτικό υγρό, τυπικά, αλλά όχι ανεξαίρετα, είναι λεμφοκυτταρικό εξίδρωμα με φυσιολογική συγκέντρωση γλυκόζης και pH. Η βιοψία υπεζωκότος έχει ευαισθησία 80% για τη διάγνωση της φυματιώδους πλευρίτιδας επειδή η παρουσία κοκκιώματος με τυροειδή νέκρωση είναι ενδεικτικό φυματιώσεως τοης υπεαζωκοτικής κοιλότητας. Η μέτρηση ADA στο πλευριτικό υγρό,είναι χρήσιμη, καθώς υψηλές τιμές είναι ιδιαίτερα συμβατές με φυματίωση, αν κια μπορεί να παρατηρηθούν ψευδώς θετικές τιμές ADA, όπως επί λεμφώματος, όμεταστατικών καρκινωμάτων, και ρευματοειδούς πλευρίτιδας. Χωρίς θεραπεία, η πλευριτική συλλογή, συνήθως λύεται, αυόματα. Εάν αφεθεί αθεράπευτη, περίπου 60% των ασθενών αναπτύσσουν φυματίωση σε άλλα όργανα-συστήματα, εντός μερικών ετών. Χορηγούνται συνήθη αντιφυματικά θεραπευτικά σχήματα και η η προσθήκη κορτικοειδών και η επιμελής παροχέτευση του υγρού βελτιώνει τα συμπτώματα αλλά ΔΕΝ μειώνει τον κίνδυνο επακόλουθης υπεζωκοτικής ινώσεως -γνωστής επιπλοκής της φυματιώδους πλευρίτιδας (βλέπε: ινοθώραξ).
Διάγνωση |εργαστηριακά ευρήματα|
--κλινικές εικόνες. Η οριστική διάγνωση απαιτεί την ταυτοποίηση του μΦ επειδή τα κλινικά ευρήματα της νόσου δεν είναι ειδικά. Από τα πλέον συνήθη συμπτώματα, της πνευμονικής φυματιώσεως, ο χρόνιος βήχας, οι νυκτερινοί ιδρώτες, η ανορεξία και η απώλεια βάρους. Αεπικονιστικά παράγονται σωρεία φαινοτύπων φυματιώσεως, που εκτείνονται από την εντελώς πειορισμένη αποτιτανωμένη ή μη εστία του gohn, μέχρι τη λίαν εκτατμένη, [ενδεχομένως] αμοφερόπλευρη, ενεργό, σπηλαιώδη φυματίωση και την κιρρωτική φυματίωση, την κλασική εικόνα της "κλαίουσας ιτέας".
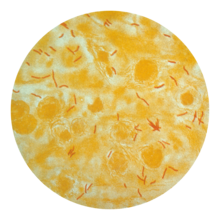 Εικόνα 2. οξεάντοχα μΦ. χρώση ziel Nielsen.
Εικόνα 2. οξεάντοχα μΦ. χρώση ziel Nielsen.
Η διάγνωση εξαρτάται από την εγρήγορση του ιατρού, ο οποίος πρέπει να έχει κατά νου την πολυμορφική εμφάνιση της φυματιώσεως, και να διεξάγει όλες τις απαραίτητες εξετάσεις, όπως η απλή χρώση πτυέλων για οξεάντοχα, όπως και καλλιέργειες σε ειδικό στερεό θρεπτικό υλικό Lowestein Jensen, σε ασθενείς με επίμονα συμπτώματα ή παθολογική ακτινογραφία θώρακος. Απαιτείται υψηλός βαθμός υπόνοιας σε άτομα που έχουν πρόσφατα μεταναστεύσει από χώρες με υψηλό δείκτη διαμολύνσωες, και σε ΄τομα υπό υψηλό κίνδυνο μολύνσεως είτε διότι διαβιούν με ασθενείς ή διότι εμφανίζουν προβλήματα ανοσοκαταστολής. ΠΑ΄ρ όλο τόι η φυματίωση συχνόερα προσβάλλει τους πνεύμονες, πρέπει να μη διαφεύγει το γεγονός ότι μπορεί να επινεμηθεί κάθε όργανο και η διάγνωση πρέπει να συνυπολογίζεται σε κάθε ασθενή με πυρετό άγνωστης αιτιολογίας. όπως και σε ασθενείς με ανώδυνες χρόνιες βλάβες στα οστά, στους νεφρούς ή τους λεμφαδένες. Ο όρος κεγχροειδής φυματίωση αναέρεται σε μια παθολογική κατάσταση όπου έχει επισυμβεί αιματογενής διασπορά της φυματιώσεως, που απεικονίζεται ως κεχρία στην ακτινογραφία θώρακος. Η αναγώριση των κεχρίων δεν είναι πολύ ευχερής και χρειάζεται η ενταχθεί σε ευρεία διαφοροδιαγνωστική λίστα, μαζί με άλλες παθολογικές καταστάσεις και παρόμοια εικόνα. Τα αναπνευστικά συμπτώματα είναι, συνήθως, ήπια, και, τυπικλα, ο ασθενής εμφανίζει χαμηλή πυρετική κίνηση, με αναιμία και απώλεια βάρους.
--εργαστηριακή διάγνωση. Η ταυτοποίηση του μΦ μπορεί να απαιτήσει μεγάλο χρονικό διάστημα ενώ η αντιφυματική αγωγή μπορεί να πρέπει να αρχίσει άμεσα, επί τη βάσει των κλινικοαπεικονιστικών ευρημάτων, ενώ αναμένονται τα αποτελέσματα των εργαστηριακών εξετάσεων. Με την υποψία της εξετάσεως πρέπει να διενεργούνται άμεσες μικροσκοπήσεις των πτυέλων, μετά χρώση Ziel Nεelsen -που αποτελεί μξέθοδο για ανίχνευση οξεάντοχων βακτηριδίων, στην οποια εμφανίζονται ως ερυθρά ραβδία (βλέπε εικόνα 2). Οι καλλιέργειες πτυέλων απαιτούν ειδικό καλλιεργητικό υπ΄στρωμα, όπως προειπώθηκε, και το μΦ αναπτύσσεται βραδέως, και χρειάζεται περίπου 4-7 εβδοομάδες, και πρόισθετες 3 εβδομάδες για την διενέργεια δοκιμασιών ευαισθησίας. Η βιοψία προσβεβλημένου οργάνου, όπως ο υπεζωκός, οι προσιτοί λεμφαδένες, το ήπαρ, ή ο μυελός των οστών, μπορεί να εμφανίσει το χαρακτηριστικό εύρημα του κοκκιώματος με τρυοειδή νέκρωση, που παράγεται με κεντρική νέκρωση, λόγω επιδράσεως των μακροφάγων, λεμφοκυττάρων και επιθηλιακών κυττάρων, εν αντιθέσει με την έκκεντρη νέκρωση και το ρυπαρό τοίχωμα που είναι χαρακτηριστικό τακέντος νεοπλάσματος, μάλλον. Τα βιοπτικά δείγματα πρέπει να προωθούνται για καλλιέργεια για μΦ, επίσης. Σημειώνεται ότι διατίθενται νέςς μέθοδοι για τη διάγνωση της φυματιώσεως που είναι ταχύτερες, ενώ εμφανίζουν μεγαλύτερη ευαισθησία και ειδικότητα. Το bactec radiometric system, π.χ., που είναι ένα υγρό μέσον που εμπεριέχει 14 C, που απελευθερώνει 14 CΟ2 όταν μεταβολίζεται και η ανίχνευσή του αποδεικνύει την παρουσία μΦ. Τεχνικές που χρησιμοποιούν το DNA, όπως η polymerase chain reacton (PCR) έχουν ήδη αναπτυχθελί και διατίθενται, με τις οποίες μπορεί να ανιχνευθτεί το μΦ σε υποστρώματα, όπως το ΕΝΥ, επί περιπτώσεων φυματιώσδους μηνιγγίτιδας. Οι τεχνικές DNA fingerprints, έχουν καταστήσει ευχερή τη διάκριση μεταξύ διαφόρων σελεχών του μΦ. Με τη μέθοδο αυτή μπορεί να διακριθεί μια αναμόλυνση από μια αναζωπύρωση σε διαφορετικούς πληθυσμούς. Εξαιτίας του αργού ρυθμού ανάπτυξης του μυκοβακτηριδίου της φυματίωσης, οι μοριακές τεχνικές έχουν αποκτήσει θεμελιώδη ρόλο στην ταχεία διάγνωση της νόσου. Έχοντας εξελιχθεί σε πλήρως αυτοματοποιημένες δοκιμασίες, οι μέθοδοι που στηρίζονται στον πολλαπλασιασμό του γενετικού υλικού (ΝΑΑΤs) είναι σε θέση να δώσουν αποτέλεσμα σε μία ή δύο μέρες, ή ακόμη και σε λίγες ώρες από την λήψη του δείγματος στο εργαστήριο. Επιπρόσθετα, η ανάγκη για έγκαιρη ανίχνευση της αντοχής στα αντιφυματικά φάρμακα, οδήγησε στην ανάπτυξη και εφαρμογή γονοτυπικών μεθόδων που ανιχνεύουν την παρουσία μεταλλάξεων που συνδέονται με αυτήν, ακόμη και στο κλινικό δείγμα. Η αντοχή στα κυριότερα αντιφυματικά φάρμακα και ιδιαίτερα στην ριφαμπικίνη, μπορεί εύκολα να ελεγχθεί με μοριακό τρόπο μιας και η συντριπτική πλειοψηφία των μεταλλάξεων εντοπίζεται σε περιορισμένες περιοχές του γονιδιώματος του βακίλου. Μέχρι σήμερα, δύο εμπορικά διαθέσιμες μέθοδοι, οι οποίες στηρίζονται στον ανάστροφο υβριδισμό σε ταινίες, έχουν υιοθετηθεί από τον ΠΟΥ. Οι μέθοδοι αυτές ανιχνεύουν τις πιο κοινές μεταλλάξεις στη ριφαμπικίνη (INNO-LiPA Rif/TB) ή και στην ισονιαζίδη (GenoType MTBDRplus). Πρόσφατα αναπτύχθηκε και υιοθετήθηκε από τον ΠΟΥ, ένα τεστ (Xpert MTB/RIF), που επιτρέπει την ταυτόχρονη ανίχνευση του βακίλου και της αντοχής του στην ριφαμπικίνη, η οποία μπορεί να χρησιμοποιηθεί ως δείκτης της πολυανθεκτικής φυματίωσης (MDR-TB).
Η βιβλιογραφία σε σχέση με τη διαγνωστική ακρίβεια των NAATs ανέρχεται σε χιλιάδες δημοσιεύσεις. Τα εμπορικά τεστ εμφανίζουν μεγαλύτερη σταθερότητα σε σχέση με τις in-house τεχνικές. Οι μετα-αναλύσεις έδειξαν υψηλή ειδικότητα μεν, χαμηλότερη και με υψηλή διακύμανση ευαισθησία δε. Στην πιο πρόσφατη από αυτές [3] η αθροιστική ευαισθησία υπολογίστηκε 0.85 (εύρος 0.36-1.00) και η ειδικότητα 0.97 (εύρος 0.54-1.00). Τα NAATs’ έχουν γενικά χαμηλότερη ευαισθησία στα έξω-πνευμονικά και μικροσκοπικά αρνητικά δείγματα. Βάσει των παραπάνω δε συνιστάται η πλήρης υποκατάσταση των κλασικών μικροβιολογικών τεχνικών από τις μοριακές μεθόδους. Τα τεστ ανάστροφού υβριδισμού, συμπεριφέρονται εξαιρετικά όσον αφορά την ανίχνευση αντοχής στη ριφαπικίνη, αλλά με μικρότερη ευαισθησία στην ισονιαζίδη δεδομένου ότι ενέχονται μεταλλάξεις περισσότερων γενετικών τόπων, που δεν ανιχνεύονται από τα τεστ. Στα άμεσα κλινικά δείγματα και κυρίως στα μικροσκοπικά θετικά, η συμπεριφορά των τεστ παραμένει εξαιρετική [4]. Τέλος, όσον αφορά την πρόσφατη τεχνική, που συνδυάζει την ανίχνευση του βακίλου ταυτόχρονα με την αντοχή στην ριφαμπικίνη, η μέχρι τώρα βιβλιογραφία, επιδεικνύει πολύ ενθαρρυντικά αποτελέσματα, ακόμη και σε «δύσκολα» περιστατικά όπως π.χ. εξω-πνευμονικής ή, παιδιατρικής φυματίωσης και HIV συν-λοίμωξης [5]. Τα NΑATs έχουν επιταχύνει κατά πολύ τόσο την διάγνωση της φυματίωσης, όσο και της αντοχής της στα κύρια αντιφυματικά φάρμακα. Πιστεύεται ότι οι ραγδαίες επιστημονικές και τεχνολογικές εξελίξεις θα επαναστατικοποιήσουν έτι περαιτέρω το πεδίο στο άμεσο μέλλον.
Μέθοδοι ανίχνευσης παραγωγής ιντερφερόνης-γ (IGRAs)
Οι μέθοδοι ανίχνευσης παραγωγής ιντερφερόνης (IGRAs) αποτελούν σχετικά νέα εργαλεία διάγνωσης της λανθάνουσας φυματίωσης. Πρόκειται για εξετάσεις ολικού αίματος, οι οποίες προσδιορίζουν την παρουσία ειδικών Τ-λεμφοκυττάρων ευαισθητοποιημένων στα αντιγόνα του M. tuberculosis. Δύο εμπορικές μέθοδοι είναι διαθέσιμες: η μέθοδος QuantiFERON-TB Gold In-Tube (QFT-GIT) (Cellestis Ltd., Australia) και η μέθοδος T-SPOT-TB (Oxford Immunotec, UK). Οι μέθοδοι αυτές αναπτύχθηκαν για τη διάγνωση της λανθάνουσας φυματίωσης, ωστόσο ερευνάται η χρήση τους και στη διάγνωση της ενεργού νόσου. Η αποτελεσματικότητα των IGRAs εξακολουθεί να είναι υπό αμφισβήτηση. Σε σύγκριση με την δερμοαντίδραση Mantoux, οι IGRAs δεν επηρεάζονται από προηγηθέντα εμβολιασμό με BCG και έκθεση στα άτυπα μυκοβακτηρίδια, λόγω των επιλεγμένων αντιγόνων-στόχων για τη διέγερση της κυτταρικής ανοσίας. Οι IGRAs δε θα πρέπει να αντικαταστήσουν τις κλασικές διαγνωστικές μεθόδους διάγνωσης της ενεργού νόσου, καθώς ένα αρνητικό αποτέλεσμα δεν αποκλείει την ενεργό φυματίωση. Όσον αφορά στη διάγνωση της λανθάνουσας φυματίωσης, οι IGRAs θα πρέπει να χρησιμοποιούνται σε συνδυασμό με τη συνολική εκτίμηση κινδύνου, για την αναγνώριση των ατόμων που πρέπει να λάβουν προφυλακτική αγωγή (πχ. παιδιά, ανοσοκατασταλμένοι, στενές επαφές ασθενών, πρόσφατη έκθεση στη νόσο κλπ.).
To σύνδρομο Waterhouse-Friedman συνιστά αιμορραγική αδρεναλίτιδα, που απολήγει σε ανεπάρκεια επινεφριδίων, λόγω αδυναμίας τους να παράξουν αλατοκορτικοειδή και προκαλείται από άλλες λοιμώξεις, επίσης, όπως από τον μηνιγγιτιδόκοκκο, την ψευδομονάδα, τον σταφυλόκοκκο, το αιμόφιλο της γρίππης, τη ναϊσέρια της μηνιγγίτιδας και τον κυτταρομεγαλοϊό. Η προφύλαξη γίνεται μέσω των αντίστοιχων εμβολίων και η θεραπεία με υψηλές δόσεις πενικιλλίνης και υδροκορτιζόνης.
βιβλιογραφία
1. Steingart KR, Henry M, Ng V, Hopewell PC, Ramsay A, et al. Fluorescence versus conventional sputum smear microscopy for tuberculosis: a systematic review. Lancet Infect Dis 2006; 6: 570-581.
2. Cruciani M, Scarparo C, Malena M, Bosco O, Serpelloni G, Mengoli C. Meta-analysis of BACTEC MGIT 960 and BACTEC 460 TB, with or without solid media, for detection of mycobacteria. J Clin Microbiol 2004; 42(5): 2321-2325.
3. Ling DI, Flores LL, Riley LW, Pai M. Commercial nucleic-acid amplification tests for diagnosis of pulmonary tuberculosis in respiratory specimens: meta-analysis and meta-regression. PLoS One 2008, 3(2):e 1536.
4. Ling DI, Zwerling AA, Pai M. Rapid diagnosis of drug-resistant TB using line probe assays: from evidence to policy. Expert Rev Respir Med 2008; 2: 583- 588.
